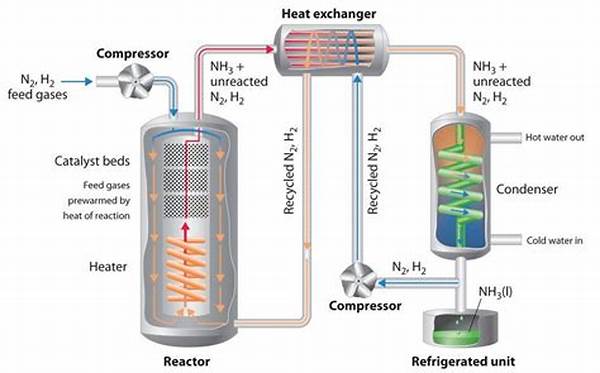
Proses Haber-bosch
Proses Haber-Bosch adalah metode industri penting yang digunakan untuk mensintesis amonia (NH₃) dari gas nitrogen (N₂) dan hidrogen (H₂). Proses ini dikembangkan oleh Fritz Haber dan disempurnakan untuk skala industri oleh Carl Bosch pada awal abad ke-20. Penemuan ini menjadi salah satu tonggak penting dalam sejarah kimia karena memungkinkan produksi pupuk nitrogen dalam skala besar, yang pada akhirnya merevolusi pertanian dunia.
Amonia yang dihasilkan melalui proses ini digunakan terutama dalam pembuatan pupuk nitrogen, yang meningkatkan hasil pertanian secara drastis dan membantu mengatasi krisis pangan global. Selain itu, amonia juga menjadi bahan baku untuk berbagai produk industri seperti bahan peledak, plastik, dan obat-obatan.
Reaksi Kimia dalam Proses Haber-Bosch
N2(g)+3H2(g)↔2NH3(g)ΔH=−92,4 kJ/mol\text{N}_2 (g) + 3\text{H}_2 (g) \leftrightarrow 2\text{NH}_3 (g) \quad \Delta H = -92,4 \, \text{kJ/mol}
Reaksi ini adalah eksotermis, artinya melepaskan panas. Namun, karena reaksi ini reversibel dan memiliki laju reaksi yang lambat pada suhu kamar, dibutuhkan kondisi khusus agar berjalan efisien di industri.
Kondisi Operasi
-
Tekanan tinggi: 150–300 atm
-
Suhu tinggi: 400–500°C
-
Katalis: Besi (Fe) dengan promotor seperti kalium oksida dan aluminium oksida
-
Rasio gas: Nitrogen dan hidrogen dalam rasio 1:3
Tahapan Proses Secara Umum
-
Produksi Hidrogen
Biasanya dari gas alam (metana) melalui proses reforming uap. -
Pemurnian Gas
Menghilangkan pengotor seperti sulfur dan karbon dioksida. -
Pencampuran dan Kompresi
Gas nitrogen dan hidrogen dicampur dalam rasio ideal, lalu dikompresi. -
Reaksi dalam Reaktor Haber
Campuran gas dialirkan melalui reaktor berisi katalis untuk membentuk amonia. -
Pendinginan dan Pemisahan
Amonia cair dipisahkan dari sisa gas, yang kemudian didaur ulang.
Dampak dan Signifikansi
-
Revolusi Pertanian: Memberi dasar bagi pupuk nitrogen modern dan mendukung pertumbuhan populasi global.
-
Kontribusi Industri: Digunakan dalam produksi urea, asam nitrat, bahan peledak, dan plastik.
-
Energi Intensif: Proses ini menyumbang sekitar 1–2% konsumsi energi global dan menghasilkan emisi karbon yang signifikan.
-
Inovasi Kimia Hijau: Penelitian terkini fokus pada alternatif proses yang lebih ramah lingkungan, seperti katalis baru dan kondisi operasi rendah energi.
Kesimpulan
Proses Haber-Bosch adalah tonggak sejarah dalam kimia industri, mengubah nitrogen dari udara menjadi amonia — senyawa penting bagi kehidupan modern. Meskipun sangat bermanfaat dalam mendukung ketahanan pangan, proses ini juga menghadapi tantangan besar dalam hal keberlanjutan energi dan lingkungan. Oleh karena itu, inovasi ke depan diarahkan untuk membuatnya lebih hijau dan efisien.